Wissenschaft

Kleiner Organismus, großes Potenzial
Ein Beitrag von Anastassija Sheremet
Extremophile Pilze nennt man Fungi, die unter extremen Lebensbedingungen, wie der trockenen Wüstenlandschaft oder in der kalten Tiefe des Meeres, gedeihen können. Diese sind für die Forschung besonders interessant, denn es wird angenommen, dass diese Organismen in extremen Lebensverhältnissen deshalb überleben können, weil sie, bediingt durch den Umweltstress, besondere Stoffe produzieren. Diese wiederum stellen für die Pharmazie großes Potenzial dar, neue medizinische Wirkstoffe entwickeln zu können. Das Labor von Frau Prof. Dr. Teusch am Institut für Pharmazeutische Biologie und Biotechnologie der HHU widmet seine Forschung genau diesem Thema.
Im Laufe der pharmazeutischen Geschichte haben Pilze immer wieder eine grundlegende Rolle bei der Entdeckung wichtiger Medikamente gespielt, die heute nicht mehr wegzudenken sind: Zum Beispiel die Entdeckung des Antibiotikums Penicillin aus dem Schimmelpilz Penicillium notatum; des Lovastatins, welches als Cholesterinsenker eingesetzt wird oder des Cyclosporins, welches bei der Organtransplantation zur Senkung der Immunreaktion dient.
Auch für die Krebsforschung sind die aus dem Organismus gewonnenen Stoffe interessant, nicht zuletzt weil auch die Nachfrage nach natürlichen Produkten in der Pharmazie groß ist. Besonders extremophile Pilze sind noch nicht stark erforscht. Im Labor von Frau Prof. Dr. Teusch an der HHU werden solche Pilze auf nützliche Wirkstoffe hin untersucht, so z.B. der marine Pilz Aspergillus chevalieri.
Kurz lässt sich ein möglicher (und hier verfolgter) Ansatz der pharmazeutischen Forschung so beschreiben: Neue Pilze werden entdeckt und ihre Extrakte isoliert. Diese unbekannten Stoffe werden auf ihre biologischen Aktivitäten hin überprüft, wozu sie teils in verschiedene andere Labore und Testzentren weitergeschickt werden. Daraus können dann möglicherweise neue Medikamente hergestellt werden. Aber wie genau funktioniert das und was passiert im Labor?

Der Prozess
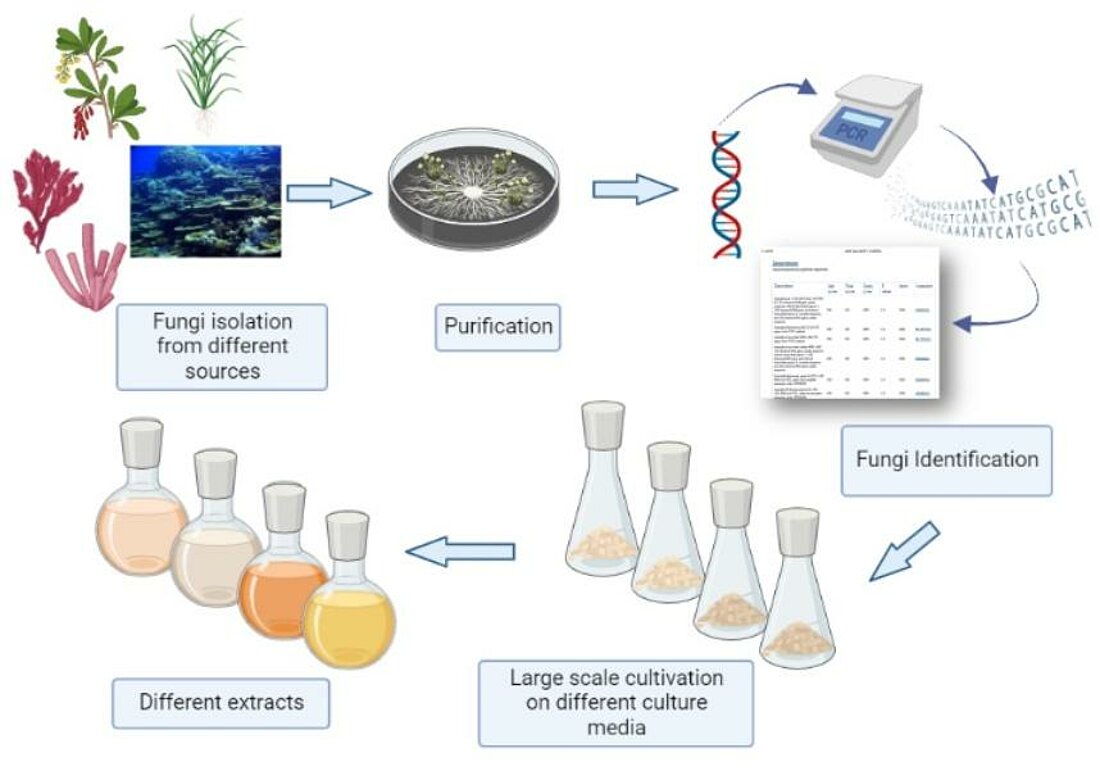
Die gesammelten Proben werden nach der Aufreinigung und der Identifikation durch biogenetische Techniken zunächst zur Gewinnung größerer Masse auf verschiedenen Nährböden kultiviert. (Dies sind im Labor von Frau Prof. Dr. Teusch entweder Reis oder Bohnen.) Die Freisetzung der für die Forschung interessanten Stoffe erfolgt durch die Induktion von gezieltem Umweltstress – zum Beispiel wird die Umgebungstemperatur, die der des nativen Habitats entspricht, verändert. Anschließend werden die Extrakte aus den Kulturen isoliert.
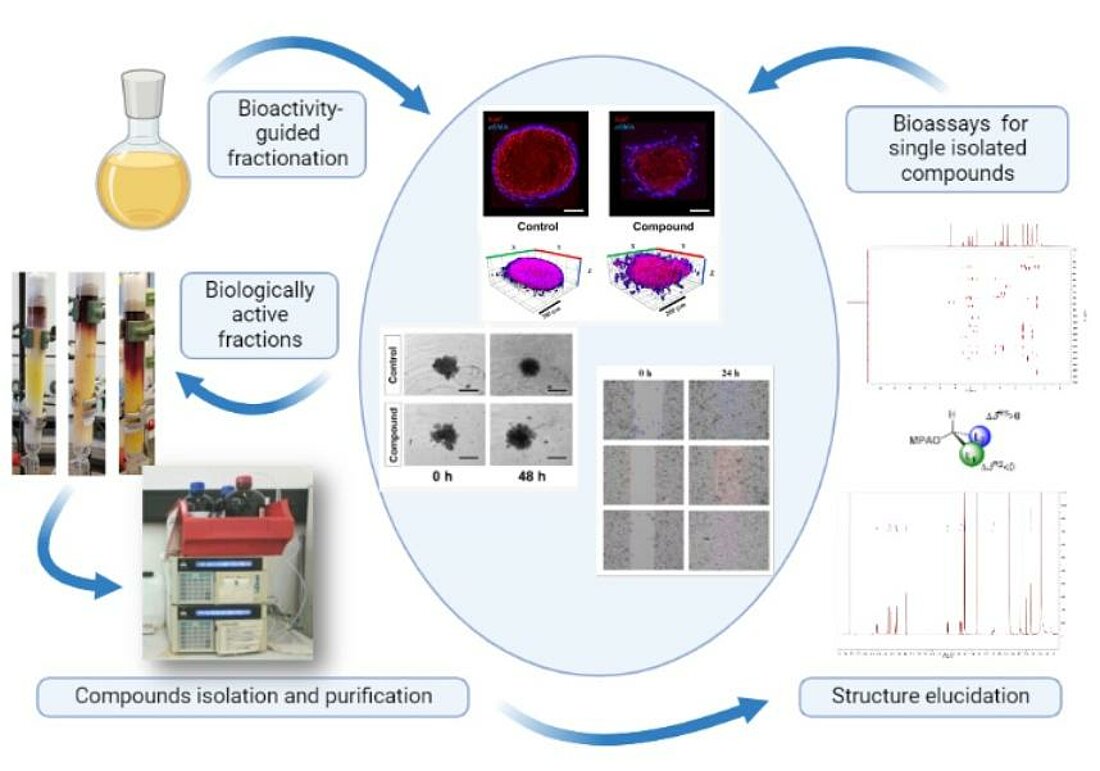
Im nächsten Schritt erfolgt die „Fraktionierung“: Hier werden die Komponenten des Pilzextrakts durch unterschiedliche Methoden aufgetrennt, so z.B. nach Größe und Polarität. Diese sogenannten „fractions“ – Teile des Extrakts – werden auf ihre Bioaktivität durch sog. Bioassays geprüft. Daraufhin erfolgt die genaue Identifikation und Charakterisierung der Stoffe durch spektrometrische Methoden wie die NMR-Spektroskopie. Denn die Aktivität der Stoffe hängt u.a. auch stark von der Konformation der Moleküle ab – also davon, wie die einzelnen Atome innerhalb des Moleküls angeordnet sind. Schlussendlich wird geprüft, auf welche Weise diese Stoffe Bioaktivität zeigen: z.B. wird auf die Cytotoxizität in humanen Zellen getestet oder auf eine entzündungshemmende Wirkung. Teilweise werden die Proben dann an andere spezialisierte Labore abgegeben.
Hier hört die Forschung des Labors von Frau Dr. Teusch am Institut für Pharmazeutische Biologie und Biotechnologie der HHU noch nicht auf. In zwei weiteren spannenden Projekten werden Modelle für die Testung der neu gefundenen Stoffe entwickelt.
Modell Krebszelle (PDAC Project)
Der Krebs der Bauchspeicheldrüse – auch Pankreaskarzinom oder auf Englisch Pancreatic ductal adenocarcinoma (PDAC) – stellt eine besonders aggressive und chemotherapeutisch schwer zu behandelnde Form der Krankheit mit hoher Sterblichkeitsrate dar. Dies ist vor allem auf die physiologisch veränderte Form der Mikroumgebung der Tumorzellen zurückzuführen: Hier kann u.a. eine vergrößerte Menge an Fibroblasten festgestellt werden. Fibroblasten sind teilungsaktive Zellen des Bindegewebes, die beim Krebs jedoch um die Tumorzellen herumliegen und die Wirksamkeit der Chemotherapie verringern.Die Bösartigkeit und Invasivität von Tumorzellen wird erhöht, wenn diese einen Prozess – genannt epithelial-mesenchymale Transition, kurz EMT – durchlaufen, welche die Zellen befähigt, zu wandern und mehr Schaden anzurichten.
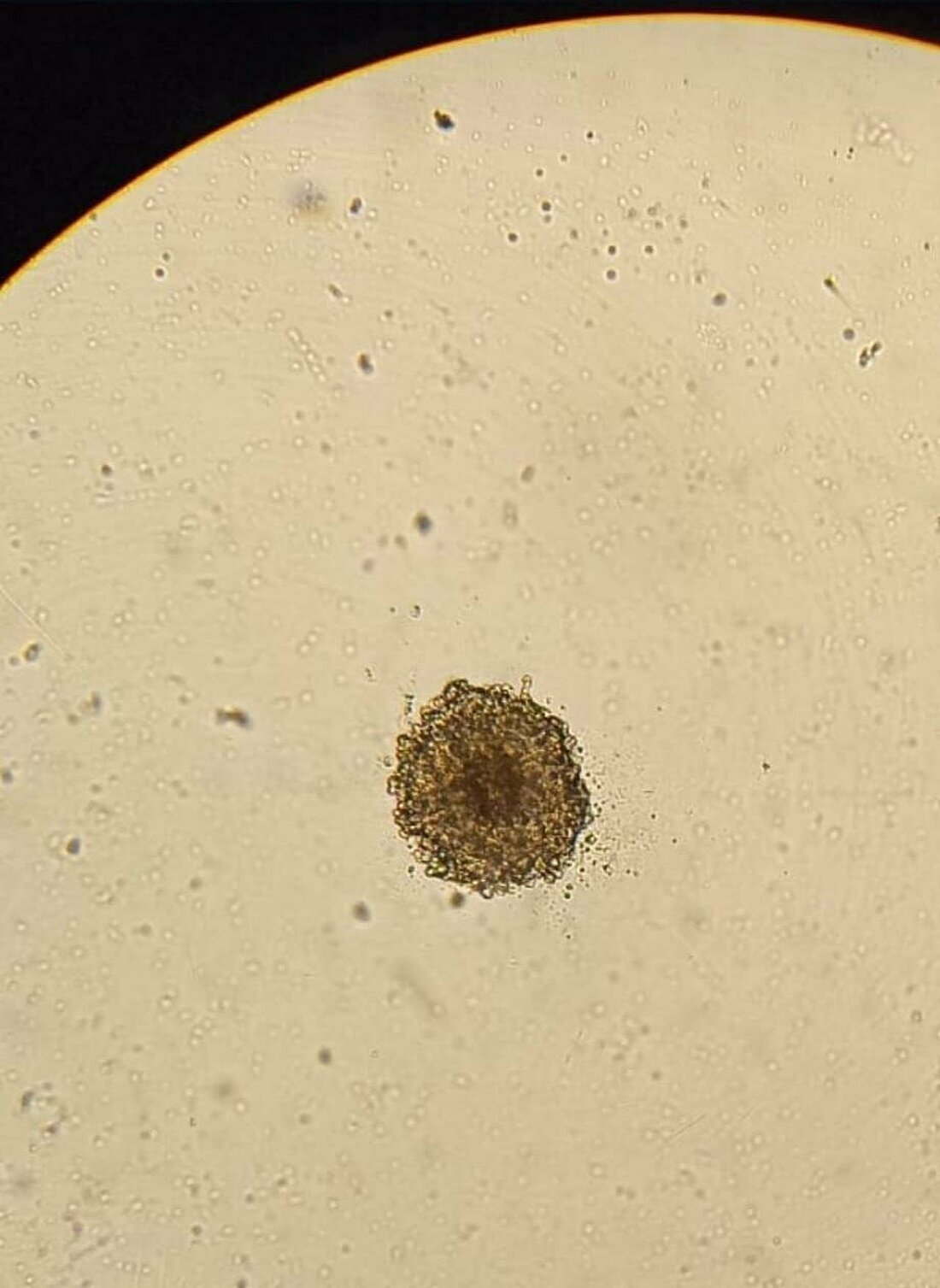
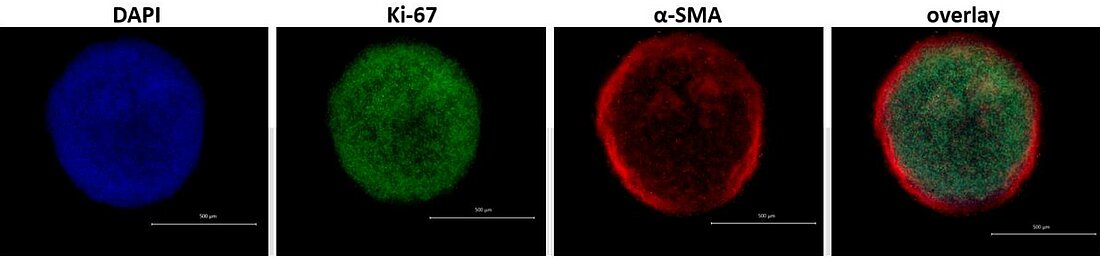
Ein vielversprechender Ansatz ist es, diese Entwicklung der Mobilität umzukehren und die Anfälligkeit der Zellen für medikamentöse Stoffe zu erhöhen. Zur Testung möglicher Stoffe im Labor wird in diesem Projekt ein Modell zur Simulation solcher typischen Tumorzellen des Bauchspeicheldrüsenkrebses entwickelt: Sogenannte „3D Spheroide“ bestehen aus PDAC Zellen und sind umhüllt von einer Schicht aus Krebspatienten stammenden Fibroblasten. Unter dem Mikroskop sieht es so aus:
Modell Haut (3D ImmunoSkin)
Die Haut ist als größtes Organ und unsere äußerste Schutzbarriere permanent und als erstes von Umwelteinflüssen wie Strahlung und Chemikalien betroffen. Deshalb ist es wichtig, die Schädigung der Haut und die Wirkung neuer Arzneimittel auf und durch diese hindurch zu verstehen.
Ein weiteres Modell soll die Haut und Blutgefäße simulieren: Dabei handelt es sich wirklich um einen kleinen, auf den ersten Blick unscheinbar aussehenden Chip, der jedoch eine Fülle an in verschiedene Schichten eingebetteten Bestandteilen aufweist: Hier werden durch kontrollierbare, kleinste Mikrokanäle Poren nachgeahmt. Bei der Testung mit Wirkstoffen lösen die eingebetteten Langerhanszellen wie in der lebenden Haut eine Immunreaktion aus. An diesem kontrollierten Modell werden genaue Wirkungswege der Stoffe (sog. pathways) mit den Zellen der Haut erforscht. Auch die oben beschriebenen Spheroide können in den Chip eingebettet werden. Der 3D Chip ermöglicht nicht nur eine kontrollierte Versuchsumgebung, sondern erlaubt auch eine Alternative zu Tierversuchen.

Allgemein ist der Weg zu wissenschaftlichen Erkenntnissen und Entdeckungen ein langer. Von der Entwicklung einer Fragestellung bis zur Testung einer Theorie sind es kleinschrittige und langwierige Prozesse, die durchlaufen werden. Jedes dieser einzelnen Forschungsthemen ist ein wichtiger Baustein, der zu einem wissenschaftlichen Durchbruch beiträgt und Fortschritt möglich macht.
Mehr zur Forschung vom Labor von Frau Dr. Teusch findet man hier.



